12月14日訊 12月10日晚間,醫(yī)保局在對曾文明等5位人大代表關(guān)于“關(guān)于將罕見病用藥納入醫(yī)保目錄的建議”提案建議的回復(fù)中給出了官方回應(yīng):
國家集中帶量采購已實現(xiàn)從試點(diǎn)到全國擴(kuò)圍和常態(tài)化運(yùn)行,下一步將把包括罕見病用藥在內(nèi)的更多品種納入集采。
符合條件的罕見病藥品基本已全部被納入了基本醫(yī)療保險支付范圍。部分價格特別昂貴的特殊罕見病用藥,由于遠(yuǎn)超基金和患者承受能力,無法被納入基本醫(yī)保支付范圍。
而目前已有一個罕見病用藥品種進(jìn)入集采,并成功降價超過80%,未來還有哪些罕見病用藥可能會進(jìn)集采呢?
01 第一個進(jìn)集采的罕見病用藥:安立生坦
值得注意的是,第一個進(jìn)集采的罕見病用藥、治療肺動脈高壓的安立生坦中選價格從115.97元/片下降到20元/片。公開資料顯示,2019年12月公布的第二批集采入圍名單中,安立生坦最高限價80元/片,中標(biāo)企業(yè)分別為華海藥業(yè)報價最低20元/片和豪森22.9元/片,未中標(biāo)企業(yè)正大天晴報價58.9286元/片,原研GSK報價70.654元/片。
據(jù)悉,國內(nèi)肺動脈高血壓的發(fā)病率在0.01%~0.02%左右,若按照我國14億人口計算,國內(nèi)大約有14萬患者。
豪森的安立生坦于2017年6月按新注冊分類4類申報上市獲受理,2018年7月31日獲上市批準(zhǔn)。2019年5月正大天晴的安立生坦也按新注冊分類4類獲上市批準(zhǔn)。
GBI Health數(shù)據(jù)顯示,截至目前,除GSK原研外,已有華海藥業(yè)、豪森以及正大天晴三家通過一致性評價。集采前,2018年最低中標(biāo)價為119.33元/5mg,仿制藥相繼上市后,2019年最低中標(biāo)價為79.33元/5mg。
那么,全國集采擴(kuò)圍與常態(tài)化運(yùn)行下,還有哪些罕見病用藥品種有可能進(jìn)集采呢?
02 有可能進(jìn)集采的罕見病用藥品種
在GBI Health數(shù)據(jù)庫中,若以“中國減稅罕見病藥品(2019年藥監(jiān)局等部分發(fā)布的首批21個減稅罕見病用藥清單)”為篩選條件,一共可以篩選出21個品種,25個劑型。其中,已經(jīng)通過一致性評價或是在一致性評價審評中的品種共計6種(青霉胺與利魯唑并未開展一致性評價),包括安立生坦、馬昔騰坦、尼達(dá)尼布、麥格司他、吡非尼酮以及曲前列尼爾。
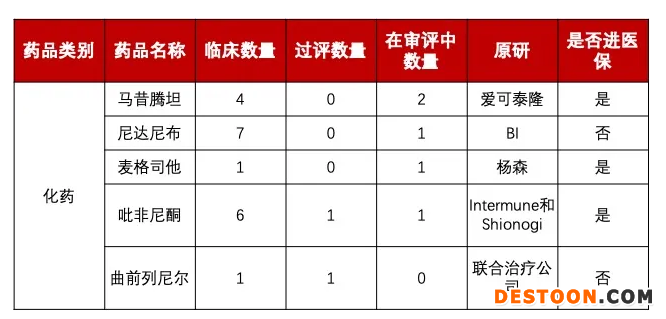
符合進(jìn)集采條件的罕見病化藥,數(shù)據(jù)來源:GBI Health
值得注意的是,除了安立生坦外,原研+過評最多的為吡非尼酮,用以治療特發(fā)性肺纖維化。
據(jù)悉,吡非尼酮由美國Intermune和日本鹽野義(Shionogi)共同開發(fā),首先于2008年10月16日獲PMDA批準(zhǔn)上市,之后于2011年2月28日獲EMA批準(zhǔn)上市,后又于2014年10月15日獲FDA批準(zhǔn)上市,由鹽野義在日本上市銷售,由Intermune在美國和歐洲上市銷售,在2013年12月25日,由北京康蒂尼藥業(yè)獲國家藥監(jiān)局批準(zhǔn)生產(chǎn)上市銷售,商品名艾思瑞,適應(yīng)癥為特發(fā)性肺間質(zhì)纖維化的治療。
數(shù)據(jù)顯示,截至目前,已有北京凱因科技一家企業(yè)過評,山東方明藥業(yè)在審評中,另有山東百諾醫(yī)藥、上海睿星基因、康恩貝、南京華威醫(yī)藥、陜西合成藥業(yè)以及成都高新區(qū)藥工醫(yī)藥生物技術(shù)研究所等6家已進(jìn)入臨床。
除了化藥外,生物藥即將進(jìn)集采也是業(yè)界共識,有哪些罕見病用生物藥符合進(jìn)集采的條件呢?



 110102000668(1)號
110102000668(1)號