1月19日訊 剛剛結(jié)束的2020年,突發(fā)的新冠疫情、接踵而來的醫(yī)藥政策,給國內(nèi)藥企帶來機遇與挑戰(zhàn)。作為國內(nèi)知名民營藥企,揚子江在過去的一年收獲滿滿:13個重磅新品獲批,攪局350億市場,26個品種通過或視同通過一致性評價(累計過評品種數(shù)46個);仿制藥申報NO.1,37個新品申報上市,其中6大品種搶首仿;17個品種申報一致性評價,7大品種搶首家過評。
13個重磅新品獲批,46個過評品種霸屏
米內(nèi)網(wǎng)數(shù)據(jù)顯示,以狀態(tài)開始時間計,2020年國家藥監(jiān)局共批準了714個國產(chǎn)仿制藥批文(仿制3/4/6類,不含原料藥),涉及250個品種(以藥品名稱計),中國生物制藥、齊魯制藥、科倫藥業(yè)、東陽光藥、揚子江藥業(yè)獲批仿制藥品種數(shù)位列前五。
2020年揚子江有13個仿制藥獲批上市,均以新注冊分類報產(chǎn),獲批生產(chǎn)后視同通過一致性評價,其中恩替卡韋口服液為劑型首仿+首家過評,左氧氟沙星滴眼液為首家過評。
表1:2020年揚子江獲批上市的品種
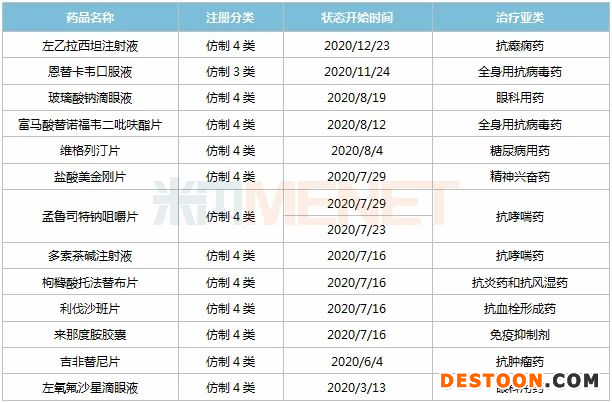
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
米內(nèi)網(wǎng)數(shù)據(jù)顯示,揚子江獲批的13個仿制藥(以通用名計)在2019年中國城市公立醫(yī)院、縣級公立醫(yī)院、城市社區(qū)中心以及鄉(xiāng)鎮(zhèn)衛(wèi)生院(簡稱中國公立醫(yī)療機構(gòu))終端市場規(guī)模超過350億元;受疫情、國家集采等因素影響,13個藥品2020上半年市場規(guī)模接近120億元。
恩替卡韋口服液為劑型首仿,目前國內(nèi)已上市的恩替卡韋主要為口服常釋劑型(片劑、分散片及膠囊劑),已被納入4+7集采,在中國公立醫(yī)療機構(gòu)終端銷售峰值超過85億元;左氧氟沙星滴眼液首家過評,目前6個滴眼液已有企業(yè)通過或視同通過一致性評價,揚子江獨占2個。
在一致性評價方面,2020年共有517個受理號以補充申請方式通過一致性評價,涉及205個品種(以藥品名稱計),揚子江藥業(yè)、上藥集團、石藥集團、中國生物制藥、復(fù)星醫(yī)藥躋身TOP5,其中揚子江以13個過評品種與上藥集團并列首位。
表2:2020年揚子江過評品種
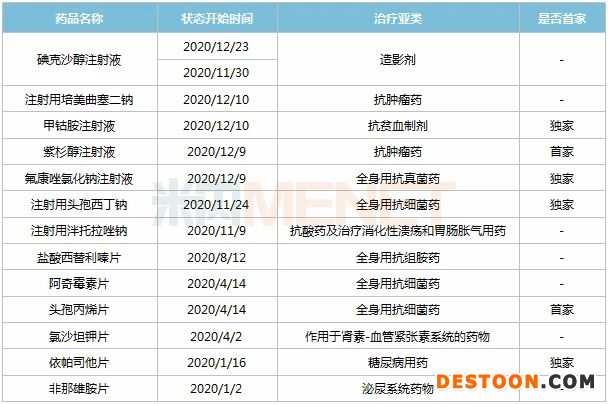
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
在一致性評價方面,揚子江專攻臨床大品種,2020年過評的13個品種中有8個在2019年中國公立醫(yī)療機構(gòu)終端的市場規(guī)模超過10億元,注射用泮托拉唑鈉、注射用頭孢西丁鈉、注射用培美曲塞二鈉銷售額超40億。
13個品種中有6個為首家過評,其中甲鈷胺注射液、氟康唑氯化鈉注射液、注射用頭孢西丁鈉、依帕司他片為獨家過評。自化學(xué)藥注射劑一致性評價正式啟動后,揚子江注射劑一致性評價迎爆發(fā)期,2020年11-12月已有7款注射劑通過一致性評價。
截至1月13日,揚子江已有46個品種通過或視同通過一致性評價,其中30個品種以補充申請方式過評,15個品種以新分類報產(chǎn),獲批生產(chǎn)后視同過評,非那雄胺片涵蓋兩種過評方式;46個品種中有18個為首家過評,其中甲鈷胺注射液、氟康唑氯化鈉注射液、注射用頭孢西丁鈉、恩替卡韋口服液、依帕司他片、鹽酸特拉唑嗪膠囊、枸櫞酸他莫昔芬片為獨家過評。
仿制藥申報NO.1,6大品種搶首仿
2020年CDE承辦受理的國產(chǎn)仿制藥申請受理號共968個(仿制3/4/6類,不含原料藥),涉及382個品種(以藥品名稱計),揚子江以37個品種領(lǐng)跑,石藥、中國生物制藥、齊魯、科倫躋身TOP5。
表3:2020年揚子江申報上市的仿制藥
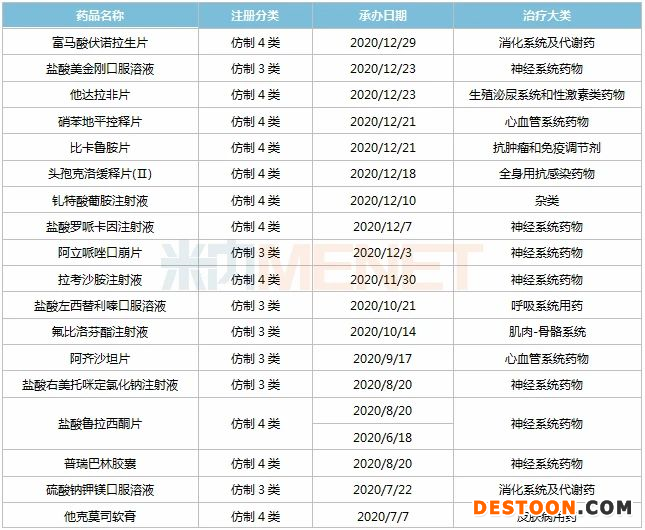
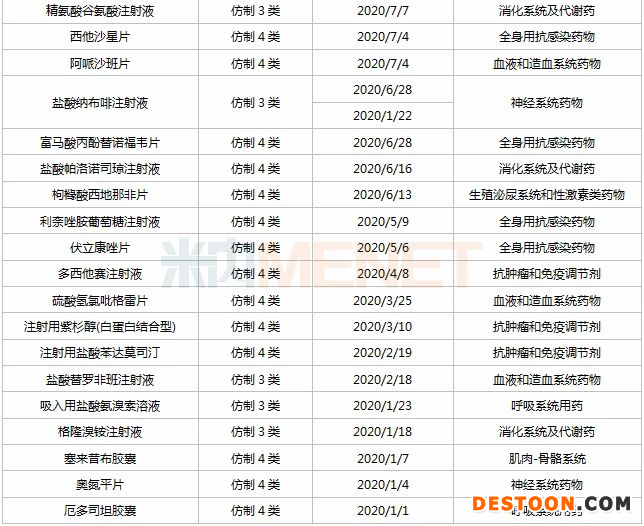
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
米內(nèi)網(wǎng)數(shù)據(jù)顯示,2020年揚子江申報上市的37個仿制藥均按新注冊分類申報,獲批生產(chǎn)后將視同通過一致性評價。從治療類別看,37個品種有11個為神經(jīng)系統(tǒng)藥物,消化系統(tǒng)及代謝藥及全身用抗感染藥物均為5個。
阿齊沙坦片、鹽酸右美托咪定氯化鈉注射液、硫酸鈉鉀鎂口服溶液3個品種在國內(nèi)市場暫時空白,富馬酸伏諾拉生片、鹽酸魯拉西酮片、西他沙星片3個品種暫未有首仿獲批上市,其中硫酸鈉鉀鎂口服溶液由揚子江獨家以新分類報產(chǎn)。
17個品種申報一致性評價,7大品種搶首家
2020年CDE承辦受理的一致性評價補充申請受理號共915個,涉及348個品種(以藥品名稱計),上藥集團以20個申報品種領(lǐng)跑,揚子江以17個申報品種緊接其后。
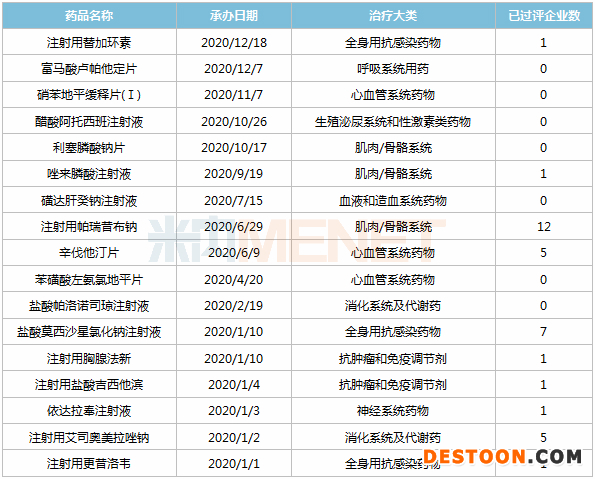
表4:2020年揚子江獲得承辦的一致性評價補充申請
來源:米內(nèi)網(wǎng)MED2.0中國藥品審評數(shù)據(jù)庫
注射劑是揚子江主攻的劑型之一,17個一致性評價申請中有12個為注射劑,且多數(shù)為臨床大品種,如注射用替加環(huán)素、注射用胸腺法新、注射用鹽酸吉西他濱、依達拉奉注射液、注射用艾司奧美拉唑鈉等。
7個品種暫無企業(yè)通過或視同通過一致性評價,其中富馬酸盧帕他定片、利塞膦酸鈉片由揚子江獨家申報,有望拿下首家過評。米內(nèi)網(wǎng)數(shù)據(jù)顯示,2019年中國公立醫(yī)療機構(gòu)終端富馬酸盧帕他定片銷售額超過2億元,同比增長37.39%,揚子江市場份額超八成。
來源:米內(nèi)網(wǎng)數(shù)據(jù)庫
注:數(shù)據(jù)統(tǒng)計截至1月13日,如有疏漏,歡迎指正!



